POPULÁCIÓGENETIKA
Kisdi Éva
ELTE Genetikai Tanszék
A populációgenetika célja a populációk genetikai összetételének vizsgálata és a genetikai összetételt változtató mechanizmusok tanulmányozása. A genetikán belül a populációs nézőpont, módszertanilag pedig a matematikai modellek alkalmazása különbözteti meg. A populációgenetika kulcsszerepet kap az evolúcióbiológiában, hiszen elemi evolúciós lépésnek egy populáció genetikai összetételének megváltozását tekintjük. Gyakorlati szempontból a populációgenetika fontos szerepet játszik például a humángenetikában (öröklődő rendellenességek előfordulása), vagy a természetvédelemben (genetikai diverzitás megőrzése).
A jelen fejezetben arra törekszünk, hogy a matematikai apparátus mellőzésével, heurisztikus módon nyújtsunk rövid bepillantást a populációgenetika alapjaiba. Kvantitatív összefüggéseket - a genetikai összetétel alapvető leírásának kivételével - csak a kiegészítő ("apróbetűs") anyagban adunk. Az érdeklődő olvasó a fejezet végén felsorolt populációgenetikai tankönyvekből tájékozódhat részletesebben.
1. A populációk genetikai összetételének leírása
Genotípus- és allélgyakoriságok
Egy populáció genetikai összetételét a populációban előforduló allélek és genotípusok gyakoriságaival írhatjuk le. Egy két alléllel rendelkező autoszómás lokuszt vizsgálva legyen az A1A1 genotípusú egyedek előfordulási aránya D, az A1A2 genotípusúaké H, az A2A2 genotípusúaké pedig R (D+H+R=1; l. 1. ábra). A D, H, R genotípus-gyakoriságok kiszámolásához csak arra van szükség, hogy minden egyednek egyértelműen meg tudjuk állapítani a genotípusát. Intermedier vagy kodomináns öröklésmenet esetén ez nem jelent problémát. Domináns-recesszív öröklődésnél viszont a heterozigótákat nem lehet megkülönböztetni a domináns homozigótáktól, ezért a genotípus- és allélgyakoriságokat csak közvetve lehet meghatározni (l. Hardy-Weinberg eloszlás).
A genotípus-gyakoriságok ismeretében könnyen kiszámolhatjuk az egyes allélek gyakoriságait is. A1 allélek az A1A1 homozigótákban és a heterozigótákban fordulnak elő; az A1A1 homozigóták minden allélja A1, de a heterozigótákban csak az allélek fele A1. Ezért az A1 allél gyakorisága p=D+H/2; hasonlóan, az A2 allél gyakorisága q=R+H/2. A két allél gyakoriságának összege természetesen 1, vagyis q=1-p.

Hardy-Weinberg eloszlás
Ha a populációban a párosodás (a vizsgált lokusz tekintetében) véletlenszerű, akkor az allélgyakoriságok alapján megadhatjuk a genotípusok gyakoriságát a létrehozott zigóták között. A1A1 zigóta csak akkor jön létre, ha egy A1 petesejtet egy A1 hímivarsejt termékenyít meg. A petesejtek p hányada A1; ezeknek ismét p hányada találkozik A1 hímivarsejttel. A keletkező zigótáknak tehát p×p=p2 hányada lesz A1A1 genotípusú. Heterozigóták létrejöhetnek úgy, hogy egy A1 petesejtet egy A2 hímivarsejt termékenyít meg (ez az összes zigóta p×q hányadában történik így), de úgy is, hogy egy A2 petesejt találkozik egy A1 hímivarsejttel (a zigóták q×p hányada). A heterozigóták gyakorisága ezért p×q+q×p=2pq lesz. Végül az A2A2 homozigóták A2 petesejtek és A2 hímivarsejtek egyesüléséből jönnek létre, gyakoriságuk q2 (az A1A1 homozigóták p2 gyakoriságával analóg módon).
Ha a három genotípus gyakorisága megfelel az imént kapott D=p2, H=2pq, R=q2 arányoknak, akkor a populáció Hardy-Weinberg eloszlást mutat. Véletlenszerű párosodás esetén a zigóták mindig Hardy-Weinberg eloszlásúak, így a Hardy-Weinberg eloszlástól való esetleges eltérés nem véletlenszerű párosodási rendszerre hívja fel a figyelmet. A felnőtt egyedek genotípus-gyakoriságai azonban pl. szelekció miatt is eltérhetnek a Hardy-Weinberg eloszlástól.
A domináns-recesszív öröklésmenetet mutató jellegeknél nem lehet közvetlen leszámolással megállapítani a három genotípus gyakoriságát, hiszen a domináns homozigótákat fenotípusuk alapján nem lehet megkülönböztetni a heterozigótáktól: csak az A1A1 és A1A2 genotípus együttes gyakoriságát (D+H), illetve az A2A2 recesszív homozigóták R gyakoriságát lehet megadni. Ilyenkor feltételezzük, hogy a populáció Hardy-Weinberg eloszlású, és az R=q2 összefüggésből határozzuk meg a q (illetve p=1-q) allélgyakoriságot. A Hardy-Weinberg eloszlás tesztelésére azonban nincs lehetőség.
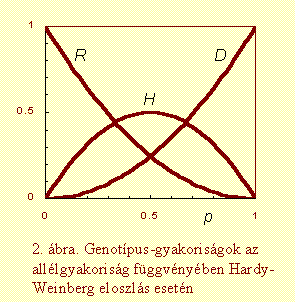 A
Hardy-Weinberg eloszlás legfontosabb tulajdonságait leolvashatjuk, ha a
három genotípus
p2, 2pq, q2
gyakoriságát ábrázoljuk az allélgyakoriság függvényében (2. ábra). Ha az
A1
allél ritka (p kicsi), akkor A1A1 homozigóták
nagyon
ritkán fordulnak elő (p2 igen kicsi): két eleve ritka
allél nagyon ritkán kerül egy egyedbe. A ritka
A1 allélek
túlnyomó része A2 allélekkel találkozik, így heterozigótákban
található. Ugyanez igaz az A2 allélre, ha az
A2
allél q gyakorisága kicsi (vagyis az A1 allél
p=1-q
gyakorisága nagy). Heterozigótákból akkor van sok, ha mindkét allél elég
gyakori, az allélgyakoriságok p=0.5,
q=0.5 körüliek.
A
Hardy-Weinberg eloszlás legfontosabb tulajdonságait leolvashatjuk, ha a
három genotípus
p2, 2pq, q2
gyakoriságát ábrázoljuk az allélgyakoriság függvényében (2. ábra). Ha az
A1
allél ritka (p kicsi), akkor A1A1 homozigóták
nagyon
ritkán fordulnak elő (p2 igen kicsi): két eleve ritka
allél nagyon ritkán kerül egy egyedbe. A ritka
A1 allélek
túlnyomó része A2 allélekkel találkozik, így heterozigótákban
található. Ugyanez igaz az A2 allélre, ha az
A2
allél q gyakorisága kicsi (vagyis az A1 allél
p=1-q
gyakorisága nagy). Heterozigótákból akkor van sok, ha mindkét allél elég
gyakori, az allélgyakoriságok p=0.5,
q=0.5 körüliek.Kapcsoltsági egyensúly és rekombináció
Az eddigiekben a populáció genetikai összetételét egyetlen lokusz szempontjából jellemeztük. Két (vagy több) lokusz együttes vizsgálatakor az első kérdés az, hogy az egyik lokuszon vett genotípus korrelál-e a másikon vett genotípussal: pl. az A1A1 egyedek között gyakoribb-e a B1B1 genotípus, mint mondjuk az A2A2 egyedek között, vagy az A1 allélt hordozó gaméták gyakrabban hordoznak B1 allélt, mint az A2 gaméták. Ha nincs ilyen korreláció a lokuszok között, akkor azt mondjuk, hogy a lokuszok kapcsoltsági egyensúlyban vannak. Ilyenkor egy gaméta pA valószínűséggel hordoz A1 allélt, és ettől függetlenül pB valószínűséggel rendelkezik B1 alléllel: az A1B1 gaméták gyakorisága tehát pApB. Ha a lokuszok nincsenek kapcsoltsági egyensúlyban, akkor az A1 gaméták gyakrabban (vagy ritkábban) hordoznak B1 allélt, az A1B1 gaméták gyakorisága eltér a pApB szorzattól. A kapcsoltsági egyensúlytól való eltérés mértéke az ún. linkage disequilibrium (D), melyet úgy számítunk ki, hogy az A1B1 gaméták tényleges gyakoriságából levonjuk a pApB szorzatot.
Véletlenszerűen párosodó populációkban a linkage disequilibrium a rekombináció révén fokozatosan csökken. Ha pl. egy A1B2 kromoszóma rekombináción megy át, akkor az A1 allél mellé pB valószínűséggel kerül B1 allél a homológ kromoszómáról, így az A1B1 kromoszómák gyakorisága közelít pApB-hez. Ha a két lokusz szorosan kapcsolt, akkor ritkán történik közöttük rekombináció és a linkage disequilibrium sokáig fennmarad. Még különböző kromoszómákon található lokuszok esetén is csak 50% a rekombináns gaméták gyakorisága, ezért független lokuszoknál D minden generációban feleződik.
A kapcsoltsági egyensúlytól való eltérést okozhatja szelekció (ha bizonyos allélkombinációk kedvezőek a szelekció során), genetikai sodródás vagy nem véletlenszerű párosodás. Az is lehetséges azonban, hogy a linkage disequilibriumhoz vezető ok már megszűnt, csak nem volt még elég idő a kapcsoltsági egyensúly beállásához. Tartósan megmaradó linkage disequilibrium a rekombináció akadályozottságára utalhat: pl. kromoszóma-inverziók akadályozzák meg, hogy a rekombináció szétzilálja a koadaptált génkomplexeket ("szupergének"). A kromoszómán fizikailag közel levő lokuszok között gyorsan beálló kapcsoltsági egyensúly arra vall, hogy a két lokusz között nagy rekombinációs gyakoriságot mutató "forró pont" található.
2. Mikroevolúciós mechanizmusok
Milyen mechanizmusok változtathatják meg egy populáció allélgyakoriságát? Induljunk ki egy zigótákból álló populációból, ahol az allélgyakoriság p. A zigóták közül némelyek megérik a felnőttkort, párosodnak és utódokat hoznak létre a mendeli hasadási arányok szerint; közben egyedek ki- és bevándorolhatnak a populációba, s az ivarsejtek képződése során mutáció is történhet. Ha (i) nincs szelekció, azaz az egyedek azonos eséllyel érik meg a felnőttkort és azonos számú utódot képesek létrehozni, (ii) nincs mutáció, (iii) nincs migráció és (iv) a populáció mérete nagy, így nincs genetikai sodródás (mintavételi hiba), akkor a felnőttekben és az általuk létrehozott gamétákban az allélgyakoriság még mindig a kiindulási p érték. Ha (v) a párosodás véletlenszerű, akkor az utódnemzedék zigótái Hardy-Weinberg eloszlást követnek, allélgyakoriságuk pedig D+H/2 = p2+pq = p(p+q) = p - vagyis egy teljes generációváltás után az allélgyakoriság változatlan. Más szavakkal, a mendeli öröklődés (meiózis és a gaméták véletlenszerű kombinációja) az allélgyakoriságot nem változtatja meg (Hardy-Weinberg törvény). Az allélgyakoriság akkor változhat meg, ha a fenti (i)-(v) feltételek valamelyike nem áll fenn.
A gyakran használt Hardy-Weinberg egyensúly kifejezés alatt hol a Hardy-Weinberg törvényt és Hardy-Weinberg eloszlást értik együttesen, hol pedig csak a Hardy-Weinberg eloszlást.
Szelekció
Ha a különböző fenotípusú egyedek más-más valószínűséggel érik meg a felnőttkort, vagy szaporodáskor különböző számú utódot tudnak létrehozni, akkor a fenotípusok rátermettsége (fitnesse) különböző. Ha egy allél nagyobb rátermettséget biztosít, akkor az őt hordozó egyedeknek több leszármazottjuk lesz, akikbe örökítik a kedvező allélt: így a kedvező allél elterjed a populációban. A kedvezőtlen alléllel rendelkező egyedek viszont kevesebb utódot produkálnak, tehát a rossz allél idővel eltűnik. A szelekció a jó allélek elterjesztése révén a jelleg adaptálódásához vezet: a rendelkezésre álló változatkészletből (lehetséges mutánsokból) a legjobb terjed el. Egyszerű példaként az ipari melanizmust említhetjük. Az angol iparvidékeken a zuzmók kipusztulásával a fák kérge sötét színűvé vált, s ebben a környezetben a nyírfaaraszoló lepke (Biston betularia) fekete (carbonaria) változata kevésbé esik a madarak prédájául, mint az eredeti világos változat. A fekete színt egyetlen domináns allél alakítja ki. Ez az allél a szelekció révén elterjedt: száz évvel az első fekete lepke észlelése után a populációnak már 95%-a fekete.
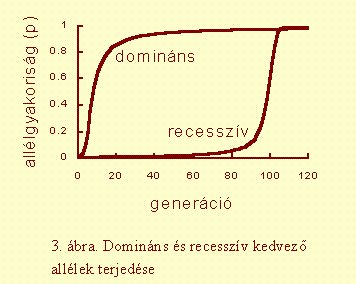
Egy allél elterjedésének (illetve eltűnésének) dinamikája attól függ, hogy az allél domináns-e vagy recesszív. Tegyük fel, hogy egy populációban mutáció révén néhány példányban megjelenik egy kedvező allél. Mivel a kedvező mutáns eleinte ritka, főleg heterozigótákban fordul elő (vö. 2. ábra). Ha domináns mutációról van szó, akkor a heterozigóták is a kedvező mutáns fenotípussal bírnak, több utódot hoznak létre, és így a kedvező mutáns allélból több kerül át a következő generációba. Ha viszont a kedvező mutáns allél recesszív, akkor hatása csak a kezdetben nagyon ritka homozigótákban nyilvánul meg, s csak ezek utódai révén kezd terjedni. Ezért a domináns jó allélek kezdetben sokkal gyorsabban terjednek, mint a recesszívek (3. ábra).
Ha egy kedvező tulajdonságot domináns és recesszív mutációk is kialakíthatnak, akkor egy domináns allél valószínűleg elterjed, mire egy recesszív mutáns észrevehető gyakoriságot érne el. Ipari melanizmust például 70 lepkefajban megfigyeltek, de csak egy esetben volt az elterjedt fekete allél recesszív, jóllehet ismeretesek fekete színt okozó recesszív mutációk is.
Egy ritka káros allél eltűnésénél hasonló különbség van a domináns és recesszív allélek között. Ha a ritka rossz allél domináns, akkor viszonylag gyorsan eltűnik, mert az őt hordozó heterozigótáknak kevés utódjuk van. A káros allélek azonban legtöbbször recesszívek. Ekkor a heterozigóták rátermettségét nem befolyásolják, s a heterozigóták átörökítik a rossz allélt az utódaikba. Csak a nagyon ritka recesszív homozigóták rátermettsége alacsony, ezért a káros allél ellen alig folyik szelekció. Egy ritka recesszív allél még akkor is nagyon lassan tűnik el végleg a populációból, ha homozigóta formában jelentős hátrányt okoz: pl. egy letális recesszív allél gyakorisága ezer generáció alatt csökken 0.001-ről 0.0005-re.
A leggyakrabban egy jó allél megléte biztosítja a nagy rátermettséget, s ilyenkor a szelekció elterjeszti a jó allélt (illetve kiirtja a rátermettséget csökkentő rossz allélt). Ha viszont a heterozigóta genotípus rátermettsége a legmagasabb, akkor nincs "jó allél". Ilyenkor a ritka allél élvez előnyt (bármelyik is az), mert a ritka allél főleg a legrátermettebb heterozigótákban fordul elő. A heterozigóta fölény tehát megakadályozza az allélek eltűnését, s ezzel védett polimorfizmust tart fenn. Ennek ismert példája a sarlósejtes vérszegénység. A sarlósejtes hemoglobin-allélre heterozigóták védettek a maláriával szemben, ugyanakkor nem szenvednek vérszegénységben sem. Ezért malária-sújtotta területeken mindkét allél jelen van a populációban. A heterozigótákat előnyben részesítő erős szelekció nagy genetikai teherrel jár: mivel a populációban szükségképpen vannak homozigóták is, elég sok ember meghal maláriában illetve vérszegénységben, ami nem lenne így, ha egy allél homozigóta formában biztosíthatná a legjobb fenotípust (maláriával szembeni védettséget vérszegénység nélkül). Ha a heterozigóták rátermettsége a legalacsonyabb (pl. inverziós kromoszómáknál), akkor a ritka allél heterozigótákban lévén hátrányba jut és eltűnik, tehát a szelekció megőrzi a már elterjedt változatot.
Mutáció
A mutáció ritka esemény (egy generációban az allélek m=10-5-10-6 -od része mutál), ezért az allélgyakoriságot egy generációváltás alatt nem változtatja meg észrevehetően. Mégsem lenne evolúció mutáció nélkül, hiszen a mutáció hozza létre az új alléleket, amelyek majd szelekció (vagy sodródás) révén elterjedhetnek.
A mutációk legnagyobb része káros allélek keletkezését (egy jól működő allél "elromlását") jelenti, s ez okozza az öröklődő rendellenességek fennmaradását: a káros alléleket a szelekció állandóan ritkítja, viszont a mutáció állandóan újra létrehozza. Egyensúlyban a mutáció ugyanannyi rossz allélt hoz létre generációnként, mint amennyi a szelekció során kiesik. A mutáns allél egyensúlyi gyakorisága nagyon kicsi: ha a mutáns allél gyakori lenne, a szelekció gyorsan csökkentené a gyakoriságát, amit a ritka mutáció nem tudna kompenzálni. Minél ritkább azonban a káros allél, annál lassabb a szelekció (különösen ha a káros allél recesszív), s egy alacsony allélgyakoriságnál a mutáció már egyensúlyt tud tartani vele (mutáció-szelekció egyensúly).
A káros mutánsok állandó jelenléte
miatt minden generációban bizonyos számú ember belehal egy öröklődő rendellenességbe
(mutációs teher). A mutációs teher nagyságát egyszerűen kiszámíthatjuk.
A populáció N egyedében 2N allél van (gyakorlatilag mind
jó allél), amelyeknek minden generációban m
hányada mutál (m
az ún. mutációs ráta). Összesen 2Nm
új mutáns allél keletkezik, tehát ennyit kell a szelekciónak kiejtenie.
Recesszív rendellenesség esetén csak a recesszív homozigóták betegek. Egy
recesszív homozigóta halála két hibás allélt távolít el a populációból,
2Nm
allél eltávolításához tehát Nm
betegnek kell meghalnia. Recesszív rendellenességeknél eszerint a populáció
m
hányada (százezred-milliomod része) hal meg egy-egy öröklődő betegségben,
a mutációs teher m.
Domináns rendellenességeknél a számítás annyiban változik, hogy a betegek
túlnyomó része heterozigóta, így egy beteg halála csak egy hibás alléltól
szabadítja meg a populációt. Ezért a generációnként létrejövő 2Nm
mutáns allélt 2Nm
beteg halála távolítja el, a mutációs teher 2m.
A fenti gondolatmenet továbbvitelével kiszámíthatjuk a mutáns allél egyensúlyi gyakoriságát is. Legyen s annak a valószínűsége, hogy egy beteg belehal a rendellenességbe (s az ún. szelekciós együttható). Recesszív rendellenességnél a populáció R=q2 hányada beteg, tehát q2s hányada hal meg; másrészt láttuk, hogy egyensúlyban a populáció m hányadának kell meghalnia. Tehát q2s=m, és innen az egyensúlyi allélgyakoriság. Ha a betegség nem túl súlyos, csak ritkán vezet halálhoz (s kicsi), akkor az egyensúlyi allélgyakoriság viszonylag magas, a betegség aránylag gyakori. A súlyos, gyakran halálos betegségeket okozó allélek viszont igen ritkák. A biztosan halálhoz vezető (letális) rendellenességek esetén s=1, és a mutációs ráta tipikus m=10-6 értéke mellett a hibás allél gyakorisága 0.001 (a rendellenesség gyakorisága q2=10-6). Domináns rendellenességek esetén a heterozigóták és a domináns homozigóták is betegek; utóbbiak azonban elhanyagolhatóan ritkán fordulnak elő. Így a betegek a populáció H=2pq hányadát teszik ki és a populáció 2pqs hányada hal bele a rendellenességbe. Egyensúlyban 2pqs=2m, és mivel a jó allél p gyakorisága alig különbözik 1-től, q jó közelítéssel m/s. A domináns mutáns allélek gyakorisága tehát jóval kisebb, mint a recesszíveké (pl. egy domináns letális mutánsé csak q=m=10-6 szemben a recesszív 0.001 gyakoriságával), mert a domináns mutánsok ellen a heterozigótákban is folyik szelekció. A betegek gyakorisága azonban nem különbözik lényegesen (domináns letális rendellenességnél 2pq=2×10-6, míg recesszív letális esetén 10-6).
Genetikai sodródás
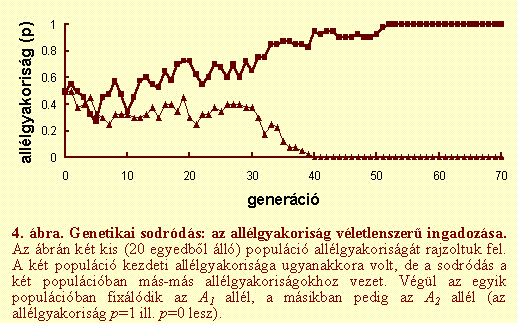 Genetikai
sodródásnak nevezzük az allélgyakoriság kis populációkban tapasztalható
véletlenszerű ingadozását (4. ábra). Ennek oka a kis populációméret miatt
bekövetkező mintavételi hiba: ha csak kevés utód születik (vagy csak kevesen
érik meg a felnőttkort), akkor ezek alléljei nem reprezentálják pontosan
a populáció eredeti genetikai összetételét. (Ha a példa kedvéért csak két
utód születne egy olyan populációban, ahol az A1 allél
gyakorisága 0.75, akkor 0.754=0.316 valószínűséggel az utódok
mind a négy allélja A1 lesz, így az A2
allél teljesen eltűnik a populációból.)
Genetikai
sodródásnak nevezzük az allélgyakoriság kis populációkban tapasztalható
véletlenszerű ingadozását (4. ábra). Ennek oka a kis populációméret miatt
bekövetkező mintavételi hiba: ha csak kevés utód születik (vagy csak kevesen
érik meg a felnőttkort), akkor ezek alléljei nem reprezentálják pontosan
a populáció eredeti genetikai összetételét. (Ha a példa kedvéért csak két
utód születne egy olyan populációban, ahol az A1 allél
gyakorisága 0.75, akkor 0.754=0.316 valószínűséggel az utódok
mind a négy allélja A1 lesz, így az A2
allél teljesen eltűnik a populációból.)
Ha a véletlen ingadozás során az egyik allél kivész, akkor a populáció tartósan szegényebb lett egy alléllel, hiszen az elveszett allél csak egy új mutáció révén jelenhet meg ismét. A sodródás tehát genetikailag "tisztítja" a populációkat, s oda hat, hogy végül csak egyfajta allél maradjon meg, azaz egy allél fixálódjon. Ha az allélek között nincs szelektív különbség, akkor a kezdetben jelenlévő allélek közül egy véletlenszerűen választott allél marad meg: egy allélfajta fixálódásának valószínűsége ezért megegyezik az allél kezdeti gyakoriságával. Ha valamelyik allél terjedését szelekció segíti, akkor persze nagyobb eséllyel fixálódik a populációban. Időnként mégis megtörténhet, hogy a sodródás révén egy szelekciós szempontból hátrányos allél terjed el: az askenázi zsidók között így válhatott gyakorivá a Tay-Sachs szindrómát okozó allél.
A különböző allélek eltűnésével, egy allél fixálódásával együtt jár a heterozigóták eltűnése is. A genetikai sodródás erősségét legegyszerűbben a heterozigóták várható gyakoriságának csökkenésével lehet jellemezni. (A várható gyakoriságot úgy képzelhetjük el, mint sok azonos méretű, elszigetelt kis populációban mért heterozigóta-gyakoriságok átlagát.) A heterozigóták várható gyakoriságát a következőképpen követhetjük nyomon. Egy véges, N egyedből álló populációban megtörténhet, hogy egy utódba ugyanannak az allélnak két másolata kerül. Ennek az esélye 1/2N, ugyanis az utód első allélja bármi lehet, 1/2N valószínűséggel pedig a második allél a 2N darab szülői allél közül pont arról másolódik, amelyikről az első. Ilyenkor az utód persze homozigóta lesz. Heterozigóta utód csak úgy jöhet létre, ha két allélja nem ugyanarról a szülői allélról másolódik (ennek esélye 1-1/2N). Ezenkívül az is szükséges, hogy a két véletlenszerűen választott szülői allél ne legyen egyforma (pl. ne két A1 allélról legyen szó): ennek valószínűsége megegyezik a heterozigóták gyakoriságával a szülők között (H). A heterozigóták várható gyakorisága az utódok között ezek szerint H' = (1-1/2N)×H. A sodródás miatt a heterozigóták annál gyorsabban fogynak el, minél kisebb a populáció: várható gyakoriságuk minden generációban (1-1/2N)-ed részére csökken.
Migráció
A populációk genetikai összetétele különbözhet azért, mert más-más allélt terjeszt el bennük a szelekció, vagy a sodródás folyamán máshogy változik bennük az allélgyakoriság. Ezzel szemben a migráció keveri a különböző populációkban található alléleket, így a populációk differenciálódása ellen hat. Ha a populációkban csak sodródás zajlik, már néhány egyed vándorlása megakadályozza a populációk genetikai differenciálódását; a sodródás szempontjából ezért egy-egy nagyobb tájegység összes egyede gyakorlatilag egy populációt alkot. Ha a populációkban eltérő allélekre folyik szelekció, migráció esetén állandóan találunk a helyi körülmények között kedvezőtlen alléleket. Nagy keveredés esetén lehetséges, hogy egy nagy populációban jó allél elterjed a szomszédos kisebb populációban is, vagy egy "generalista" fenotípust kialakító allél terjed el minden populációban.
Nem véletlenszerű párosodás
A sokféle nem véletlenszerű párosodási rendszerből itt hármat emelünk ki, hogy illusztráljuk a populáció genetikai összetételére gyakorolt hatásokat.
(1) Beltenyésztésről akkor beszélünk, ha rokon egyedek párosodnak egymással. A rokonok részben azonos alléleket hordoznak, ezért utódaik nagyobb valószínűséggel lesznek homozigóták, mint véletlenszerű párosodás mellett. Mivel sok káros allél recesszív, a rokon-házasságból származó gyermekek között több szenved valamilyen genetikai rendellenességben. Drosophilán végzett kísérletek szerint minden haploid genomban van egy recesszív letális mutáció. Mivel pl. az unokatestvérek génjeinek 1/16-a közös, unokatestvér-párosítás esetén az utód 1/16 eséllyel örökli ugyanazt a recesszív letális mutációt mindkét szülőtől. Véletlenszerű párosodás esetén ez csak 0.001 valószínűséggel következne be. A Drosophilának ugyanis kb. ezer "esszenciális" lokusza van, s a recesszív letális allélek gyakorisága mindegyiken kb. q=0.001; így egy adott lokuszon az egyedek q2=10-6 hányada recesszív homozigóta, míg az ezer lokusz valamelyikén kb. a populáció 0.001 hányada az. A beltenyésztés több homozigótát és kevesebb heterozigótát eredményez, azaz a genotípus-gyakoriságokat eltolja a Hardy-Weinberg eloszláshoz képest. A populáció allélgyakoriságát azonban a beltenyésztés nem változtatja meg.
 (2)
Szubpopuláción
belüli párosodás. Gyakran előfordul, hogy a populáció több, egymástól
többé-kevésbé izolált szubpopulációból áll, ahol egyedek többnyire a saját
szubpopulációjukon belül párosodnak. Az illusztráció kedvéért tegyük fel,
hogy két teljesen elszigetelt, egyforma nagy szubpopulációról van szó,
az allélgyakoriság legyen az egyikben p1=0.5, a másikban
p2=0.9.
Az első szubpopulációban a heterozigóták aránya
H1=2p1q1=0.5,
a másodikban
H2=2p2q2=0.18;
az egész populációban a heterozigóták gyakorisága (H1+H2)/2=0.34.
A teljes populáció allélgyakorisága (p1+p2)/2=0.7,
Hardy-Weinberg eloszlás esetén ennek 2×0.7×0.3=0.42 heterozigóta-gyakoriság
felel meg. A heterozigóták tényleges gyakorisága (0.34) azonban ennél kisebb:
a teljes populáció nem Hardy-Weinberg eloszlású, jóllehet az egyes szubpopulációk
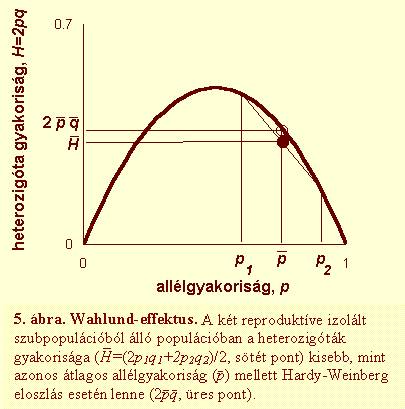
külön-külön Hardy-Weinberg eloszlást követnek (5. ábra). A szubpopulációkra
tagolt populációkban kevesebb heterozigóta (és több homozigóta) van, mintha
a párosodás az egész populációban véletlenszerű lenne. A tapasztalt jelenséget
Wahlund-effektusnak
nevezik. A Hardy-Weinberg eloszlástól való eltérés mértékével lehet jellemezni
a szubpopulációk genetikai differenciálódását: minél jobban különböznek
az egyes szubpopulációk allélgyakoriságai,
annál nagyobb a Hardy-Weinberg eloszlástól való eltérés a teljes populációban.
(2)
Szubpopuláción
belüli párosodás. Gyakran előfordul, hogy a populáció több, egymástól
többé-kevésbé izolált szubpopulációból áll, ahol egyedek többnyire a saját
szubpopulációjukon belül párosodnak. Az illusztráció kedvéért tegyük fel,
hogy két teljesen elszigetelt, egyforma nagy szubpopulációról van szó,
az allélgyakoriság legyen az egyikben p1=0.5, a másikban
p2=0.9.
Az első szubpopulációban a heterozigóták aránya
H1=2p1q1=0.5,
a másodikban
H2=2p2q2=0.18;
az egész populációban a heterozigóták gyakorisága (H1+H2)/2=0.34.
A teljes populáció allélgyakorisága (p1+p2)/2=0.7,
Hardy-Weinberg eloszlás esetén ennek 2×0.7×0.3=0.42 heterozigóta-gyakoriság
felel meg. A heterozigóták tényleges gyakorisága (0.34) azonban ennél kisebb:
a teljes populáció nem Hardy-Weinberg eloszlású, jóllehet az egyes szubpopulációk
külön-külön Hardy-Weinberg eloszlást követnek (5. ábra). A szubpopulációkra
tagolt populációkban kevesebb heterozigóta (és több homozigóta) van, mintha
a párosodás az egész populációban véletlenszerű lenne. A tapasztalt jelenséget
Wahlund-effektusnak
nevezik. A Hardy-Weinberg eloszlástól való eltérés mértékével lehet jellemezni
a szubpopulációk genetikai differenciálódását: minél jobban különböznek
az egyes szubpopulációk allélgyakoriságai,
annál nagyobb a Hardy-Weinberg eloszlástól való eltérés a teljes populációban.
A Wahlund-effektust először herbáriumi növények vizsgálata során vették észre: a herbáriumi példányok között gyakran kevesebb heterozigóta van, mint amennyi a Hardy-Weinberg eloszlás alapján várható. A a növényeket gyakran különböző élőhelyekről gyűjtötték, így azok más-más szubpopulációból vagy populációból származnak.
(3)
Autoinkompatibilitás.
Egyes növények (pl. lóhere, lucerna) úgy védekeznek az önbeporzás ellen,
hogy bibéjükön a pollen nem tud tömlőt hajtani, ha az autoinkompatibilitási
lokuszon a pollenben levő allél a bibe szövetében is megtalálható: például
egy A1A2 növényt sem A1,
sem A2 pollen nem tud megtermékenyíteni. Egy ilyen autoinkompatibilitási
rendszerben legalább három allélnak kell lennie, s valamennyi egyed heterozigóta.
Ha három meglevő allél mellett felbukkan egy negyedik mutáns allél is,
akkor ez eleinte előnyt élvez: mivel ritka, az őt hordozó pollenszemcsék
gyakorlatilag minden egyedet megtermékenyíthetnek. Az új mutáns allél tehát
terjedni kezd. Ugyanígy terjedni fog az ötödik, hatodik stb. mutáns is;
ezeknek a növényeknek egy-egy populációjában száz különböző allél is található
az autoinkompatibilitásért felelős lokuszon, ami azt jelenti, hogy jóformán
minden egyed más-más genotípusú. Az autoinkompatibilitás nemcsak a genotípus-gyakoriságokat
változtatja meg, hanem az allélgyakoriságokat is.
3. Természetes populációk genetikai polimorfizmusa
A természetes populációk genetikailag igen polimorfak: az enzimlokuszok mintegy harmadán több, gélelektroforézissel elválasztható (tehát töltésükben is különböző) enzimvariáns található, míg DNS szinten gyakorlatilag minden lokusz variábilis.
Mivel minden populáció véges méretű, valamekkora genetikai sodródás minden populációban zajlik. Ha a Hardy-Weinberg törvény többi feltétele teljesül, a sodródás miatt előbb-utóbb minden populációban az egyik allélnek fixálódnia kellene. Ez azonban nem történik így. Milyen mechanizmusok őrizhetik meg a természetes populációk óriási genetikai variabilitását?
(1)
Polimorfizmust fenntartó szelekciós
mechanizmusok. Ha a ritka allélek előnyben vannak a szelekció során
(függetlenül attól, hogy éppen melyik allél ritka), akkor a szelekció megakadályozza
az allélek eltűnését, s így védett polimorfizmust tart fenn. Ez történik
például heterozigóta fölény esetén (l. a szelekcióról szóló szakaszt);
ám heterozigóta fölényre elég kevés példát ismerünk a természetből. Vannak
azonban más polimorfizmust megőrző szelekciós mechanizmusok is. Ilyen a
heterogén, "foltos" környezetben folyó szelekció: ha például a párosodó
populáció fele olyan habitatból származik, ahol az A1
allélre folyik szelekció, míg a másik felében az A2 allélre,
akkor mindkét allél megmarad a populációban. Ugyanígy polimorfizmust tarthat
fenn az időben változó szelekció is (pl. egyes években az A1
allél jó, más években az A2).
Különböző habitatokból álló környezetben a ritka allél előnyben van, mert azt a habitatot tudja kihasználni, amelyikben kevesebb egyed osztozik az erőforrásokon. Legyen például az A1 allél ritka, tehát az A2A2 genotípus gyakori. Ekkor az első habitatban - ahol az A1 allél jó, de az A2A2 genotípus rátermettsége kicsi - kevés egyed éli túl a szelekciót, de köztük az A1 allélt hordozók nagyobb arányban lesznek. Mivel kevés túlélő van, egy egyedre sok táplálék (és más erőforrás) jut. Ezért a szelekciót túlélő egyedek fejenként sok utódot hozhatnak létre, s így sok örökli az A1 allélt is. A második habitatban ugyan az A2 allélt hordozó egyedeknek kedvez a szelekció, ám itt sok túlélő lesz, az egyes egyedekre kevés táplálék jut, és kevesebbet szaporodhatnak. Az intraspecifikus kompetícióban való különbség a ritka A1 allélt részesíti előnyben. - A ritka allél előnye időben változó szelekciónál is megmutatható. Az egyszerűség kedvéért tegyük fel, hogy egy recesszív allél általában előnyt élvez, de időnként egy járvány kipusztítja a recesszív homozigótákat. Két járvány között a recesszív allél elterjed, a ritka domináns allél heterozigótákban található. A következő járványt csak a heterozigóták élik túl, így a recesszív allél gyakorisága 0.5-re esik vissza. Ez a ciklus ismétlődik, miközben fluktuáló gyakorisággal ugyan, de mindkét allél megmarad a populációban.
Gyakoriságfüggő szelekciónál
az egyes fenotípusok rátermettsége attól függ, hogy a populációban melyik
fenotípus milyen gyakran fordul elő. Ha mindig a ritka fenotípusok előnyösek,
akkor az őket kialakító ritka allélek terjedni fognak, ami védett polimorfizmust
eredményez. Ez a mechanizmus igen sokféle ökológiai szituációban megvalósulhat.
Egyik érdekes példáját a Tanganyika-tóban élő pikkelyevő ragadozó halaknál
láthatjuk. A ragadozók szája aszimmetrikus: egyes egyedek az áldozat bal
oldalát, mások a jobb oldalát tudják megtámadni. A préda halak igyekeznek
figyelni a hátulról támadó ragadozókra. Ha a baloldalt támadó ragadozók
gyakoriak, a prédák is inkább a bal oldalukra vigyáznak: ekkor a jobboldalt
támadó ritka változat könnyebben jut prédához, így előnyt élvez. Megfordítva,
ha a baloldalt támadó fajta ritka, akkor az kerül előnybe. A száj aszimmetriáját
valószínűleg egy lokusz két allélja határozza meg, mégpedig a baloldalt
támadó fenotípus domináns. A két fenotípus egyformán gyakori a tóban, és
gyakoriságuk 11 éven át állandó volt: a gyakoriságfüggő szelekció stabilizálja
az allélek arányát. - Gyakoriságfüggő szelekció érvényesülhet a prédánál
is. Egy ritka színű vagy mintázatú préda "kieshet" a predátor keresőképéből,
és így előnyben lehet a gyakori változathoz képest. Mimikrivel rendelkező
fajoknál előnytelen az, ha túl sokan utánozzák ugyanazt a modellt (a ragadozók
nem tanulják meg elég jól, hogy az adott mintázatú állatot nem szabad megenni,
hiszen elég gyakran találkoznak az ehető utánzó fajjal is). Egy másik modellt
utánzó változat tehát előnyt élvez. S valóban, például az afrikai fecskefarkú
lepke (Papilio dardanus) egy populációjának egyedei több ehetetlen
fajt utánoznak. A mintázatot több lokusz alléljai alakítják ki. Ezek szoros
kapcsoltságban vannak (egy "szupergént" alkotnak): ezáltal elkerülhető,
hogy rekombináció révén "keverék", egyik modellre sem hasonlító mintázatok
alakuljanak ki.
A préda-predátor rendszerekhez hasonlóan a parazitákkal való koevolúció is könnyen vezethet polimorfizmushoz. A paraziták nyilván úgy evolválódnak, hogy a gazda gyakran előforduló típusait tudják hatékonyan megtámadni; a gazda ritka változatai tehát előnyben lesznek. Ugyanígy a gazdában a gyakori parazita-típusok ellen alakul ki hatékony védelem, ami a ritka parazita-fajták előnyéhez vezet. Fajon belüli kompetíciónál előnyben van az a ritka változat, amely kissé eltérő forrásokat képes hasznosítani, így a kompetíció is tarthat fenn polimorfizmust. Viselkedésökológiában is gyakran találkozunk gyakoriságfüggő szelekcióval. Lazacoknál például a nagytestű hímek tudnak sikeresen küzdeni a nőstényekért. A populációban azonban vannak sokkal kisebb hímek is, amelyek igyekeznek a nőstény közelében elbújni, hogy egy óvatlan pillanatban rábocsássák spermájukat a nőstény által kibocsátott petékre. Ha a "settenkedő" kicsik túl gyakoriak, akkor nehezen találnak üres búvóhelyet, a nyílt küzdelemben pedig alulmaradnak: ilyenkor a nagyok vannak előnyben. Ha viszont a kicsik ritkák, akkor bőven van üres búvóhely, s ekkor a kicsik jobban járnak, mint a nagyok. A kétféle stratégia öröklődik, a kicsik és a nagyok védett polimorfizmusban együtt élnek. A nem-véletlenszerű párosodási rendszerek közül például az autoinkompatibilitás is polimorfizmushoz vezet.
Szorosan kapcsolt lokuszok közül elég, ha az egyiken hat valamilyen polimorfizmust fenntartó szelekció: a többi lokusz alléljai (linkage disequilibriumban) az első lokusz alléljaihoz kötve "autóstoppal utaznak", így ezeken a lokuszokon is megmarad a polimorfizmus.
(2) Mutáció-szelekció egyensúly. A mutáció és szelekció egyensúlyában több allél van ugyan jelen, ám a szelekciós szempontból káros allélek gyakorisága igen kicsi, a legjobb allélé meg igen nagy (l. a mutációról szóló szakaszt). Konvenció szerint egy lokuszt nem tekintünk polimorfnak, ha azon egy igen elterjedt ("vad") allél mellett csak néhány nagyon ritka ("mutáns") allél van jelen. Ezért egylokuszos jellegeknél a mutáció-szelekció egyensúly nem jelent polimorfizmust. Sok lokusz által befolyásolt, kvantitatív tulajdonságoknál azonban más a helyzet: a sok lokusz valamelyikén már gyakrabban következik be mutáció, így egyensúlyban jelentős mértékű genetikai variabilitás marad fenn (vö. Kvantitatív genetika fejezet).
(3) Mutáció és genetikai sodródás egyensúlya: neutrális elmélet. Az elektroforetikusan különböző enzimvariánsok funkcionális szempontból legtöbbször egyenértékűek, ugyanazt a reakciót ugyanolyan jól katalizálják. Ilyenkor egyik allélre sem folyik szelekció, az allélek szelekciós szempontból neutrálisak. A DNS-szintű variabilitás még nagyobb része neutrális, hiszen a változatok jelentős részét teszik ki a szinonim mutációk (a mutáns a genetikai kód degeneráltsága folytán ugyanazt az aminosavat kódolja, mint az eredeti szekvencia) és a konzervatív aminosav-helyettesítések (azonos töltésű és kb. azonos méretű aminosavak cseréi, amelyek a fehérje szerkezetét nem változtatják meg). Az enzim- illetve DNS-polimorfizmus túlnyomó részénél tehát csak a genetikai sodródás és a mutáció jön számításba: a sodródás miatt időről időre egy allél elvész a populációból, míg a mutáció révén új allélek jelennek meg.
Mivel egy fehérjének sokféle neutrális változata van, az új mutáns allélek nem ugyanazok, mint a sodródás során elvesztettek. A populáció genetikai variabilitása beáll ugyan egy egyensúlyi értékre, de ebben az egyensúlyban a különböző allélek állandóan cserélődnek. Ezért nem lenne célszerű a populációt az egyes allélek gyakoriságaival jellemezni. Ehelyett az egy mintában található különböző allélek számát, illetve a (bármilyen két allélt hordozó) heterozigóta egyedek gyakoriságát használják a populáció polimorfizmusának mérésére.
 Kis
populációkban erős a genetikai sodródás, gyorsan elvesznek az allélek,
s ezeket a ritka mutációk alig pótolják: a kis populációk genetikai variabilitása
igen kicsi. Nagy populációkban viszont gyenge a sodródás, így a mutációk
révén jelentős genetikai variabilitás halmozódik fel. A polimorfizmus mértéke
függ a kérdéses fehérje szerkezetétől és funkciójától is. Ha csak kevés
aminosavat lehet úgy helyettesíteni, hogy a fehérje működése ne szenvedjen
kárt, akkor kevés neutrális mutáns keletkezik, hiszen a legtöbb mutáció
káros lesz (és ezek gyorsan eltűnnek a populációból). Ha viszont a fehérje
szerkezete sokféle aminosavcserét lehetővé tesz a funkció károsodása nélkül,
akkor a neutrális mutációk gyakorisága nagyobb. Mind az allélek száma,
mind pedig a heterozigóták gyakorisága a populáció egyedszámának (N)
és a neutrális mutációk rátájának (m)
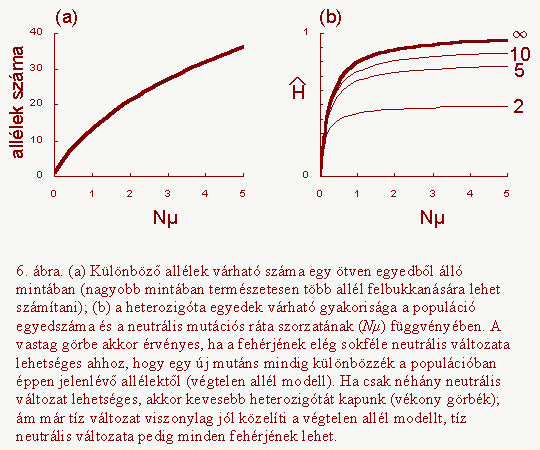
szorzatától függ (6. ábra).
Kis
populációkban erős a genetikai sodródás, gyorsan elvesznek az allélek,
s ezeket a ritka mutációk alig pótolják: a kis populációk genetikai variabilitása
igen kicsi. Nagy populációkban viszont gyenge a sodródás, így a mutációk
révén jelentős genetikai variabilitás halmozódik fel. A polimorfizmus mértéke
függ a kérdéses fehérje szerkezetétől és funkciójától is. Ha csak kevés
aminosavat lehet úgy helyettesíteni, hogy a fehérje működése ne szenvedjen
kárt, akkor kevés neutrális mutáns keletkezik, hiszen a legtöbb mutáció
káros lesz (és ezek gyorsan eltűnnek a populációból). Ha viszont a fehérje
szerkezete sokféle aminosavcserét lehetővé tesz a funkció károsodása nélkül,
akkor a neutrális mutációk gyakorisága nagyobb. Mind az allélek száma,
mind pedig a heterozigóták gyakorisága a populáció egyedszámának (N)
és a neutrális mutációk rátájának (m)
szorzatától függ (6. ábra).
A heterozigóták várható gyakoriságát egyensúlyban jó közelítéssel megkaphatjuk a következő gondolatmenet alapján. A genetikai sodródásnál láttuk, hogy a heterozigóták gyakorisága minden generációban (1-1/2N)-ed részére csökken, azaz mutáció nélkül a következő generációban csak H'=(1-1/2N)×H heterozigóta lenne. A mutációk viszont új alléleket hoznak létre, s ezzel növelik a heterozigóták gyakoriságát. Mivel egy fehérjének igen sok neutrális változata lehet, feltehetjük, hogy minden mutáció olyan új allélt eredményez, amely éppen nem volt jelen a populáció egy egyedében sem (ún. végtelen allél modell): ekkor minden utód heterozigóta, amelyikbe mutáns allél jut. Körülbelül 2m annak a valószínűsége, hogy az utódba kerülő allélek közül az egyik mutáns (mindkét allél oly ritkán mutál, hogy azt nyugodtan elhanyagolhatjuk). Ám az utód kb. H valószínűséggel mutáció nélkül is heterozigóta lett volna; a heterozigóták gyakorisága tehát csak 2m(1-H) -vel nő a mutációk révén. Mind a sodródás, mind a mutáció hatását figyelembe véve a heterozigóták várható gyakorisága az utódok között H' = (1-1/2N)×H + 2m(1-H). Egyensúlyban a heterozigóták gyakorisága állandó (H'=H=), a
egyenletből kifejezve
. Az egyensúlyi heterozigótaság tehát csak az Nm szorzattól függ; ezt a függvényt ábrázoltuk vastag vonallal a 6(b) ábrán.
Mivel természetes (nem túl kicsi)
populációkban a sodródás gyenge és a mutációk ritkák, az egyensúlyi genetikai
variabilitás igen lassan áll be. Az egyensúly eléréséhez nagyságrendben
N
generáció szükséges: egy kétmilliós populációnál (évente egy generációval
számolva) ez a pleisztocén kezdete óta eltelt időnek felel meg! Kis populációknál
azonban az egyensúly gyorsan beáll, ami azt jelenti, hogy a kis populációk
gyorsan elvesztik genetikai variabilitásukat.
 A
természetben a populációk egyedszáma jelentős változásokon mehet keresztül,
s a múltbeli egyedszámok - az egyensúly lassú beállása miatt - erősen befolyásolják
a ma megfigyelhető genetikai variabilitást. Különösen erős az átmeneti
egyedszám-csökkenés, vagyis a populáció beszűkülésének hatása. Ha a populáció
létszáma egy ideig kicsi, ez alatt az idő alatt a genetikai variabilitása
gyorsan csökken. Ezután hiába nő meg újra az egyedszám: a beszűkülés alatt
elvesztett alléleket csak a ritka mutációk pótolják, így az eredeti genetikai
variabilitás hosszú ideig nem áll helyre (ún. bottleneck-effektus;
7. ábra). Ilyen populáció-beszűkülés történhetett a gepárdok és az elefántfókák
esetében, ami miatt mindkét faj gyakorlatilag teljesen elveszítette genetikai
variabilitását.
A
természetben a populációk egyedszáma jelentős változásokon mehet keresztül,
s a múltbeli egyedszámok - az egyensúly lassú beállása miatt - erősen befolyásolják
a ma megfigyelhető genetikai variabilitást. Különösen erős az átmeneti
egyedszám-csökkenés, vagyis a populáció beszűkülésének hatása. Ha a populáció
létszáma egy ideig kicsi, ez alatt az idő alatt a genetikai variabilitása
gyorsan csökken. Ezután hiába nő meg újra az egyedszám: a beszűkülés alatt
elvesztett alléleket csak a ritka mutációk pótolják, így az eredeti genetikai
variabilitás hosszú ideig nem áll helyre (ún. bottleneck-effektus;
7. ábra). Ilyen populáció-beszűkülés történhetett a gepárdok és az elefántfókák
esetében, ami miatt mindkét faj gyakorlatilag teljesen elveszítette genetikai
variabilitását.
Az egyedszám változását technikailag úgy veszik figyelembe, hogy a tényleges egyedszámokból egy ún. effektív egyedszámot számolnak; ez az egyes generációkban mért egyedszámok harmonikus közepe (az egyedszámok reciprokai átlagának reciproka). A változó egyedszámú populáció sodródás szempontjából úgy viselkedik, mint az effektív egyedszámával egyező állandó méretű populáció. Már néhány kis érték az egyedszámok között erősen lehúzza az effektív egyedszámot: ha pl. egy populáció létszáma tíz generációból nyolcban 1000 de két generációban csak 10, akkor az effektív egyedszám mindössze 48.
A genetikai polimorfizmus
jelentősége
A genetikai variabilitás ad lehetőséget arra, hogy a populációk a jövőben adaptálódni tudjanak a (gyakran emberi behatásra is) változó környezethez. Ha a populációban többféle allél van jelen, akkor a szelekció révén mindig az az allél terjedhet el, amelyik az adott körülmények között előnyös. Ha viszont nincs genetikai variabilitás, akkor a populációnak "várnia" kell egy igen ritkán bekövetkező szerencsés mutációra, s eközben a populáció könnyen kihalhat. Egy populáció számára gyakran igen fontos a biotikus környezete (kompetitorok, predátorok, paraziták); a biotikus környezet a többi faj evolúciója révén még akkor is változik, ha a fizikai környezet nagyjából állandó marad. Így egy olyan populáció, mely nem rendelkezik a szükséges genetikai variabilitással, menthetetlenül lemaradhat például a gyorsan evolválódó parazitákkal vívott "fegyverkezési versenyben".
Nemcsak evolúciós, hanem ökológiai időskálán is hátrányban lehet egy olyan faj, amelynek alacsony a genetikai variabilitása. A variábilisabb populációk többféle élőhelyet használhatnak ki, illetve könnyebben hódíthatnak meg új élőhelyeket. A polimorf populációk a járványokkal szemben is védettebbek. Ha a populáció minden tagja ugyanarra a kórokozóra érzékeny, akkor ennek a kórokozónak megjelenése hatalmas járványhoz vezet; ha viszont egyes egyedek az egyik, mások a másik kórokozó-típussal szemben védettek, akkor egy kórokozó sem pusztít el túl sok egyedet.
Genetikai szempontból a polimorfizmus elvesztése veszélyes, mert beltenyésztéses leromlással járhat. Ennek két oka van: egyrészt a genetikai sodródás során káros allélek is rögzülhetnek a populációban, másrészt eltűnnek a heterozigóták, amelyek egyes lokuszokon esetleg a legjobb genotípust képviselik. Végül saját érdekeinket is említhetjük: a nemesítés során a természetes populációk genetikai készletéből ("génbankjából") válogatjuk ki a számunkra legmegfelelőbb változatokat.
A természetvédelem egyik fontos szempontja
a genetikai variabilitás megőrzése. A genetikai polimorfizmus elvesztése
a kicsi, elszigetelt populációkat fenyegeti. Mekkorának kell lennie legalább
egy "genetikailag életképes" populációnak? A rendelkezésre álló (elég bizonytalan)
adatok alapján úgy tűnik, hogy 5000 egyed elég a kvantitatív tulajdonságok
genetikai varianciájának megbízható fenntartásához. Ezeket a tulajdonságokat
azonban sok lokusz határozza meg, s genetikai variabilitásukhoz nem szükséges,
hogy minden egyes lokusz polimorf legyen. Egylokuszos jellegek variabilitásának
megőrzéséhez lényegesen nagyobb, százezres nagyságrendű populációra van
szükség. A "bottleneck-effektus" miatt ügyelni kell arra, hogy a populáció
elkerülje az erős beszűküléseket. A szelekció által fenntartott polimorfizmus
megmaradásához lényeges lehet az eredeti heterogén habitatszerkezet, a
"foltos" környezet megőrzése is.
A normális polimorfizmust mutató populációkban a heterozigóták átlagos gyakorisága durván 0.05 és 0.2 közé esik. A neutrális elmélet alapján a 6b ábráról könnyen leolvashatjuk, illetve aösszefüggésből kiszámolhatjuk, hogy kb. 0.1 heterozigóta-gyakorisághoz Nm-nek kb. 0.03-nak kell lennie. m=10-6 mutációs rátát feltételezve ez N=30 000 effektív egyedszámot jelent. Ám az effektív egyedszám több okból is jóval kevesebb, mint a tényleges létszám: a populációméret elkerülhetetlen ingadozásán kívül függ a korcsoportstruktúrától, az egyes szülők által létrehozott utódok számának variabilitásától, az ivararánytól és a párosodási rendszertől is. Ezért a szükséges populációméretet az effektív egyedszám öt-tízszeresére becsülik, ami már százezres nagyságrendre rúg.
4. Az adaptáció populációgenetikája
Fenotípusos optimalizáció
Az adaptáció vizsgálatakor rendszerint abból a feltételezésből indulunk ki, hogy a szelekció már elterjesztette a lehetséges allélok közül a legjobbat, így a populáció egyedei a legjobb fenotípust mutatják. A fenotípus és a rátermettség közötti kapcsolat ismeretében meghatározhatjuk az optimális fenotípust, illetve megvizsgálhatjuk, hogy különböző környezeti tényezők hogyan befolyásolják az optimumot. Eközben a genetikai részleteket (hány lokusz milyen alléljai hogyan határozzák meg a kérdéses jelleget) figyelmen kívül hagyjuk.
A fenotípusos optimalizációval szemben felhozható, hogy genetikai megkötöttségek megakadályozhatják azt, hogy a szelekció elterjessze a legrátermettebb fenotípust. Ilyen genetikai megkötöttség lehet a heterozigóta fölény vagy a rekombináció. Ha a legjobb fenotípus egy heterozigóta genotípusnak felel meg, akkor a legjobb fenotípus nem terjedhet el, hiszen nincs olyan populáció, amely kizárólag heterozigóta egyedekből állna: a heterozigóták a mendeli hasadási szabályok szerint mindig létrehoznak kevésbé rátermett homozigóta utódokat is. Hasonlóan, ha egy két lokusz által meghatározott jellegnél az A1B1 és az A2B2 kombinációk eredményeznek jó fenotípust és ezeknek kellene elterjedniük, a rekombináció miatt állandóan képződnek a hátrányos A1B2 illetve A2B1 kombinációk is. Hosszú távon azonban ezek a megkötöttségek valószínűleg eltűnnek. Heterozigóta fölény esetén felbukkanhat egy olyan új allél, amely homozigóta formában képes kialakítani a legjobb fenotípust; a koadaptált gének kromoszóma-átrendeződés révén oly közel kerülhetnek egymáshoz, hogy a rekombináció elhanyagolhatóvá válik.
Evolúciósan stabil stratégiák
Gyakoriságfüggő szelekció esetén az egyes fenotípusok rátermettsége a populáció összetételétől függ. Ilyenkor nincs értelme "legjobb" fenotípusról beszélni: csak azt kérdezhetjük, hogy egy adott populációban, az ott jelenlévő fenotípusokkal szemben mely fenotípusok rátermettek. Egy populációban újabb és újabb fenotípusok terjedhetnek el mindaddig, amíg az összes lehetséges mutáns fenotípus rátermettsége kisebb nem lesz, mint a populációban már meglevő fenotípusoké.
Egyszerű esetben van egy olyan fenotípus, amellyel szemben minden más változat hátrányban van: ha ez a fenotípus egyszer elterjedt a populációban, akkor nincs olyan új mutáns, amely terjedni tudna. Ezt a fenotípust evolúciósan stabil stratégiának (ESS-nek) nevezzük. Ha például a nőstények egy jellegzetes mintázatról, násztáncról stb. ismerik fel a hímeket, akkor bármilyen új mintázatú vagy násztáncú hím hátrányba kerül, az elterjedt fenotípus tehát ESS. Máskor nincs olyan fenotípus, amely önmagában ESS lenne, hanem több fenotípus megfelelő arányú keverékével szemben nem tud más mutáns elterjedni: ilyenkor kevert ESS-ről beszélünk. A lazacok esetében (l. a polimorfizmust fenntartó szelekciós mechanizmusoknál) nagytestűeket és kicsiket megfelelő arányban tartalmazó populációban más testméretű változatok nem terjedhetnek el; a közepesek alulmaradnának a nyílt küzdelemben a nagyokkal szemben, a rejtőzésben pedig a kicsikkel szemben.
Ha az ESS egyetlen fenotípusnak felel meg, és ezt a fenotípust egy allél homozigóta formában alakítja ki, akkor az erre az allélra fixálódott populáció evolúciósan stabil. Kevert ESS-eknél a helyzet bonyolultabb. Lehetséges, hogy a kevert ESS-t egyetlen homozigóta genotípus alakítja ki úgy, hogy az egyedek bizonyos gyakorisággal más-más fenotípust mutatnak: egyes növények például többféle méretű magot hoznak létre, de ezek a magok genetikailag teljesen egyformák. Ilyenkor továbbra sincs probléma, a kevert ESS-nek megfelelő homozigóták populációjából a szelekció minden más mutáns allélt kiejt. Ha viszont a különböző fenotípusok más-más genotípusnak felelnek meg, akkor nem biztos, hogy populációgenetikai egyensúlyban a fenotípusok aránya megfelel a kevert ESS-nek. Például az ESS lehet három fenotípus 1:1:1 arányú keveréke. Ha a három fenotípus az A1A1, A1A2 és A2A2 genotípusoknak felel meg, akkor ezek véletlenszerű párválasztás (Hardy-Weinberg eloszlás) esetén nem fordulhatnak elő 1:1:1 arányban.
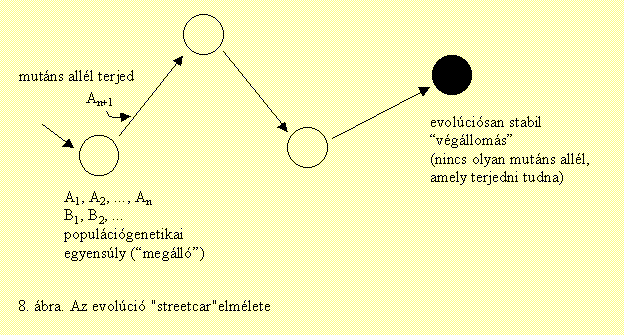 Az
evolúciósan stabil stratégiák vizsgálata nyitva hagyja azt a kérdést, hogy
a populáció valaha is fixálódik-e az ESS-t kialakító allélra, illetve több
lehetséges ESS esetén melyiket éri el a populáció. A gyakoriságfüggő szelekció
dinamikájának leírásához nyújt szemléletes képet az evolúció "streetcar"
(azaz "villamos") elmélete. Induljunk ki egy tetszőleges populációból,
ahol a vizsgált lokuszokon akárhány allél lehet (8. ábra). A jelenlévő
allélek viszonylag gyorsan populációgenetikai egyensúlyba kerülnek, gyakoriságuk
nem változik tovább: az evolúciós "villamos" megáll. A megállóból egy olyan
új mutáns allél érkezése mozdít ki, amely terjedni tud a populációban.
Az új allél terjedése miatt változnak az allélgyakoriságok (esetleg egyik-másik
allél el is tűnik), amíg újra beáll egy populációgenetikai egyensúly. Ez
a folyamat ismétlődik - a "villamos" megy, megáll, ismét megindul, ismét
megáll - amíg el nem érkezünk a "végállomáshoz", egy evolúciósan stabil
populációhoz, amelyben már egyetlen mutáns allél sem tud terjedni.
Az
evolúciósan stabil stratégiák vizsgálata nyitva hagyja azt a kérdést, hogy
a populáció valaha is fixálódik-e az ESS-t kialakító allélra, illetve több
lehetséges ESS esetén melyiket éri el a populáció. A gyakoriságfüggő szelekció
dinamikájának leírásához nyújt szemléletes képet az evolúció "streetcar"
(azaz "villamos") elmélete. Induljunk ki egy tetszőleges populációból,
ahol a vizsgált lokuszokon akárhány allél lehet (8. ábra). A jelenlévő
allélek viszonylag gyorsan populációgenetikai egyensúlyba kerülnek, gyakoriságuk
nem változik tovább: az evolúciós "villamos" megáll. A megállóból egy olyan
új mutáns allél érkezése mozdít ki, amely terjedni tud a populációban.
Az új allél terjedése miatt változnak az allélgyakoriságok (esetleg egyik-másik
allél el is tűnik), amíg újra beáll egy populációgenetikai egyensúly. Ez
a folyamat ismétlődik - a "villamos" megy, megáll, ismét megindul, ismét
megáll - amíg el nem érkezünk a "végállomáshoz", egy evolúciósan stabil
populációhoz, amelyben már egyetlen mutáns allél sem tud terjedni.
Ajánlott irodalom
Crow J.F. & M. Kimura (1970): An introduction to population genetics theory. Harper and Row, New York
Natura Kiadó, Budapest, pp. 53-82.